Sbobby
Creato da studenti, per studenti.
Carica la registrazione.
Ottieni la sbobina.
ISCRITTI
ELABORATE
PROCESSATI
Dall'audio alla sbobina completa
Non una semplice trascrizione
Sbobina
DopoCaratteristiche generali e struttura del citomegalovirus
Il citomegalovirus (CMV) è il più grande tra i virus erpetici umani, caratterizzato da un genoma a DNA a doppio filamento di circa 230.000–240.000 paia di basi, dimensioni che lo collocano all'estremo superiore della famiglia Herpesviridae. Dal punto di vista architetturale condivide la struttura tipica degli herpesvirus: capside icosaedrico, tegumento proteico e pericapside lipidico con glicoproteine di superficie; pertanto, gli elementi strutturali fondamentali non si discostano da quelli degli altri membri della famiglia.
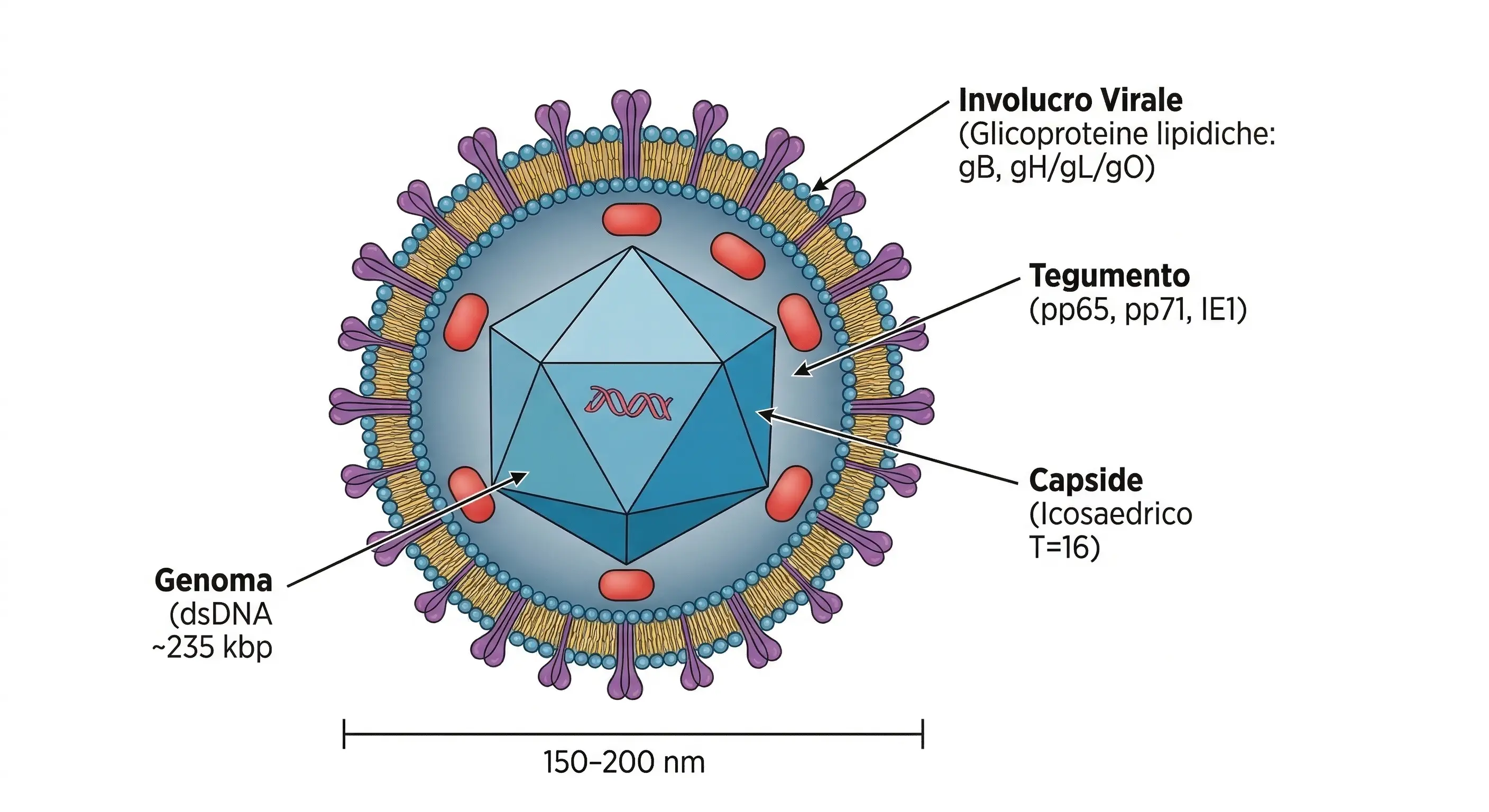
[Nota dello Sbobinatore] Nella trascrizione emerge il riferimento a "150 mila paia di basi", ma tale stima è considerata errata o quantomeno superata. Il CMV possiede il genoma più esteso tra gli Herpesviridae umani. Si precisa che il testo riporta il dato corretto (230.000–240.000 paia di basi).
Specificità d'ospite e coltivazione in vitro
Il CMV è un virus strettamente umano: infetta l’uomo e trova nell’uomo stesso il proprio reservoir naturale. Questa specificità biologica ha ricadute pratiche anche in laboratorio. In coltura cellulare, infatti, il virus presenta esigenze stringenti: non cresce efficacemente in linee cellulari immortalizzate non umane, come le Vero (derivate da rene di scimmia), ma richiede linee cellulari umane diploidi, non immortalizzate e con cariotipo conservato, per sostenere la replicazione produttiva. Questa necessità riflette l’adattamento del virus a contesti cellulari umani e la sua dipendenza da fattori dell’ospite finemente sintonizzati.
Significato del nome e alterazioni citopatiche
Il nome "citomegalovirus" deriva dalla spiccata tendenza del virus a indurre marcato aumento del volume cellulare e la formazione di sincizi di grandi dimensioni, fenomeno condiviso con altri herpesvirus ma particolarmente evidente nel CMV. Sul piano morfologico, l'infezione determina inclusioni intracellulari spesso localizzate a livello intranucleare, che conferiscono alle cellule l'aspetto classico definito "a occhio di civetta". Queste alterazioni citopatiche, osservabili in preparati istologici o in colture infette, sono utili per il riconoscimento morfologico dell'infezione e costituiscono un tratto distintivo coerente con l'etimologia del termine.
[Nota dello Sbobinatore] La trascrizione menziona genericamente inclusioni "intracellulari". Si specifica che, sebbene inclusioni citoplasmatiche possano esistere, l'aspetto diagnostico "a occhio di civetta" è dato specificamente dalla grande inclusione basofila intranucleare, circondata da un alone chiaro.
Tropismo cellulare, infezione produttiva e sedi di latenza
Il virus presenta un marcato tropismo cellulare: pur essendo un patogeno umano, è in grado di infettare numerosi tipi cellulari e, di conseguenza, può essere rilevato in molti organi e in pressoché tutti i principali fluidi biologici. Questa ampia distribuzione tissutale e nei secreti corporei riflette la flessibilità del ciclo replicativo in relazione al tipo di cellula ospite.
Infezione produttiva: cellule bersaglio e implicazioni
Quando il virus entra in cellule permissive, instaura un’infezione produttiva: il genoma virale viene espresso in maniera completa, si formano nuove particelle virali e queste vengono secrete e rilasciate, consentendo la propagazione dell’infezione ad altre cellule e potenzialmente ad altri ospiti. Le cellule in cui questo andamento è tipico comprendono i macrofagi, i fibroblasti e gli epiteli e endoteli. La produttività in questi compartimenti cellulari spiega la presenza del virus in molteplici distretti anatomici e la sua abbondanza nei fluidi biologici, facilitando sia la diffusione intraospite sia, quando le condizioni lo consentono, la trasmissione interumana.
Latenza: sedi e caratteristiche
Diversamente da virus che stabiliscono la latenza principalmente nel sistema nervoso centrale o nei gangli nervosi (come gli alfa-herpesvirus), questo patogeno adotta una latenza circolante. I principali serbatoi cellulari della latenza sono i linfociti T e i monociti, in cui il genoma virale persiste in forma quiescente. Questa scelta ecologica comporta che la latenza non sia confinata in una singola sede anatomica, ma sia diffusa nel compartimento ematico e immunitario.
Oltre al circolo periferico, è possibile rilevare il genoma virale in latenza anche nel midollo osseo, in particolare nelle cellule stromali. La presenza nel microambiente midollare, insieme al coinvolgimento di linfociti T e monociti, suggerisce un modello di persistenza che integra compartimenti circolanti e nicchie emopoietiche, offrendo al virus un vantaggio nel mantenimento a lungo termine e potenziali opportunità di riattivazione in condizioni favorevoli.
[Nota dello Sbobinatore] Si precisa che, sebbene la trascrizione menzioni anche i "linfociti B", la latenza di CMV è primariamente associata ai linfociti T e alla linea monocitica/mieloide. Il reservoir nei linfociti B è invece caratteristico di un altro herpesvirus, EBV. Il testo è stato corretto per riflettere la specificità di CMV.
Quadro clinico generale, riattivazione e presenza in liquidi biologici
Il citomegalovirus (CMV) è un patogeno di grande rilievo clinico, ma con impatto disomogeneo a seconda del profilo del paziente. È un virus altamente prevalente nella popolazione generale e, analogamente agli altri Herpesviridae, può instaurare una fase di latenza e successivamente riattivarsi. Nella maggior parte dei soggetti immunocompetenti l’infezione decorre in modo asintomatico oppure con manifestazioni lievi e aspecifiche, tanto da risultare difficilmente attribuibili in modo univoco al CMV. Questo carattere subdolo contribuisce alla sua diffusione: la presenza di sintomi non è necessaria perché si verifichi la trasmissione.
Latenza e riattivazione
Come gli altri herpesvirus, il CMV permane nell’organismo in stato di latenza dopo l’infezione primaria. Periodicamente può andare incontro a riattivazioni, durante le quali si ha produzione e secrezione di particelle virali. Queste fasi possono essere clinicamente silenti, ma sono comunque rilevanti sul piano epidemiologico, poiché i pazienti risultano infettivi anche in completa assenza di sintomatologia. La dinamica si osserva sia nei soggetti con infezione primaria recente sia in quelli con infezione pregressa e riattivata, con un profilo clinico che resta spesso modesto, a meno di condizioni predisponenti.
Presenza del virus nei liquidi e nei tessuti
Durante l’infezione, primaria o da riattivazione, il CMV può essere rilevato in numerosi liquidi biologici e tessuti. Non tutti i compartimenti risultano positivi simultaneamente, ma è frequente l’isolamento del virus in campioni diversi provenienti dallo stesso paziente. Tra i materiali in cui il CMV è tipicamente riscontrabile rientrano il liquido seminale, il liquido amniotico e le secrezioni vaginali; ciò conferma la possibilità di trasmissione per via sessuale. Questa distribuzione multisede, che può includere anche altre secrezioni e tessuti non specificati in dettaglio in questa sede, sottolinea la necessità di considerare il CMV nella diagnosi differenziale di quadri aspecifici e nella valutazione del rischio di trasmissione in differenti contesti clinici.
Trascrizione
PrimaIl citomegalovirus è il più grande dei virus erpetici che conosciamo, quantomeno di quelli umani. Con un genoma, vedete, intorno alle 150 mila paia di basi, doppio filamento di DNA, quindi a livello strutturale nulla è diverso rispetto al agli altri virus erpetici di cui abbiamo già parlato, quindi non spendo ulteriori parole per per quanto riguarda la struttura. Di specifico, il citomegalovirus è un virus umano, ha, che è un virus prettamente umano. Ok? Quindi è un virus che è in grado di infettare solo l'uomo, quindi l'uomo è il reservoir di sé stesso della malattia che che lo colpisce. Ehm anche in cultura cellulare ha bisogno di determinate condizioni per poter essere isolato e coltivato, quindi non cresce nelle classiche linee cellulari immortalizzate, tipo le Vero, che non sono cellule umane, sono cellule di scimmia, c'è bisogno di una linea umana diploide, quindi non immortalizzata, non con diciamo anomalie dal punto di vista del del cariotipo. Il nome citomegalovirus deriva dalla capacità che ha questo virus, ma abbiamo visto che ce l'hanno anche gli altri virus erpetici, questo, diciamo, particolarmente è in grado di dare sincizi molto grandi, come questo che vedete nella figura, in cui ci sono moltissimi nuclei più delle inclusioni intracellulari, a volte citoplasmatiche, a volte intranucleari. E per questo motivo è stato, appunto, chiamato citomegalovirus. E per quanto riguarda il tropismo, al di là di essere un virus umano, è in grado di infettare moltissimi tipi cellulari, ok? Per cui lo possiamo ritrovare disseminato in tutti gli organi di una persona infetta, lo possiamo trovare in tutti i fluidi biologici che espelliamo dal nostro corpo. A seconda del tipo cellulare che questo virus infetta, possiamo avere o un'infezione produttiva, quindi virus che viene secreto, viene espulso e rilasciato dalle cellule e quindi può infettare altre cellule o eventualmente altri ospiti, e questo avviene tipicamente nei macrofagi, fibroblasti e tutti gli epiteli e gli endoteli. motivo che vi spiega anche il perché sia un virus che si trova così, diciamo, profusamente in in tutti i fluidi biologici. Per quanto riguarda invece la sede di latenza, qui la distinzione rispetto ai virus che abbiamo visto l'altra volta è importante, perché non siamo più su una latenza sulle cellule del sistema nervoso centrale, ma siamo in una latenza, diciamo, circolante, quindi prevalentemente i linfociti, sia T che B, e i monociti, sono le cellule in cui questo virus va in latenza, quindi capite bene che è una latenza che non è localizzata in una singola sede, come potrebbe essere un ganglio nervoso nel caso dei degli alfa herpes virus, ma è un virus che comunque possiamo ritrovare in in in circolo e anche nel midollo, soprattutto nelle cellule stromali del midollo osseo, possiamo ritrovare il genoma del virus in latenza. Ehm, per quanto riguarda la patologia, allora, questo è un virus molto importante dal punto di vista clinico, anche se lo è solo per alcune tipologie di pazienti, in modo abbastanza simile a quello che abbiamo visto l'altra volta. Eh è un è un virus molto prevalente nella popolazione, che molto spesso è completamente asintomatico o dà delle sintomatologie molto lievi e difficilmente associabili in modo specifico all'infezione da parte del citomegalovirus. Ehm e come gli altri herpes, una volta che va in latenza, può riattivarsi, ok? Quindi può dare ciclicamente dei degli episodi di riattivazione, dei periodi di riattivazione in cui viene prodotto virus e viene secreto virus, quindi i pazienti sono infettivi, possono trasmettere il virus anche, in questo caso, in completa assenza di sintomatologia. Ehm. Qui vedete una serie di liquidi e tessuti che sono tipicamente positivi per citomegalovirus in un paziente che è in corso di infezione, che sia un'infezione primaria, che sia una riattivazione, possiamo trovare il il virus in moltissimi di questi tessuti, non per forza in tutti contemporaneamente, però in in molti casi può essere trovato davvero in in campioni diversi. Tra questi vedete che c'è liquido seminale, liquido amniotico, secrezioni vaginali, quindi è un virus che si può trasmettere anche per via sessuale. oltre alla classica via, diciamo, per contatto di mucosasa orale, scambio di saliva e liquido amniotico significa anche che è un altro virus erpetico che è in grado di dare infezione congenta. E ne parleremo poi in modo più esteso perché risulta essere il più importante virus dal punto di vista delle infezioni virali congenite, quindi quello che ha una incidenza in assoluto più elevata tra tutti i virus che conosciamo e quello che può dare anche delle patologie o può causare la morte nella diciamo, la proporzione più alta tra tutti i virus che conosciamo. Quindi è un virus che ha delle particolarità, appunto, in alcune fasce di pazienti, ma in quelle fasce va assolutamente riconosciuto prima e possibilmente gestito una volta che è stata fatta la la diagnosi.
Trascrizione grezza
Come altri tool: solo testo dall'audio
Sbobina completa
Sbobby: contenuto integrale strutturato
Integrazione slide e immagini
Carica le slide insieme all'audio. Sbobby le legge per integrare la sbobina.
- Slide e audio insieme, sbobina più ricca
- Immagini e schemi inseriti dove servono
Correzione automatica
Le "Note dello Sbobinatore" correggono imprecisioni, chiariscono termini tecnici e aggiungono contesto, rendendo la sbobina uno strumento affidabile.
[Nota dello Sbobinatore]
Nella trascrizione emerge il riferimento a "150 mila paia di basi", ma tale stima è considerata errata. Il CMV possiede il genoma più esteso tra gli Herpesviridae umani, pari a 230.000–240.000 paia di basi.
Ricerca accademica in corso
Analizzando PubMed e fonti accademiche...
Meccanismi di replicazione
Paper individuato
Viral pathobiology of Human Cytomegalovirus
Recent advances in understanding the mechanisms of HCMV replication and its interaction with the host immune system...
Terapie Antivirali (Ganciclovir)
Non fermarti alla sbobina.
Approfondisci sui paper.
Sbobby cerca su database accademici come PubMed articoli e fonti verificate sui contenuti della lezione.
Ricerca automatica
Database accademici come PubMed analizzati in tempo reale.
Concetti chiave spiegati
Approfondimenti sui termini più complessi della lezione.
Fonti verificate
Solo articoli pertinenti, con grado di rilevanza.
Un ambiente pensato
per lo studio.
Editor a blocchi per organizzare la sbobina, aggiungere note e generare riassunti in pochi secondi.
Editor a blocchi
Trascina paragrafi e immagini dove vuoi.
Riassunti personalizzati
Sintetizza i concetti più complessi.
Esportazione rapida
PDF o Word in un clic.
Lezione: Citomegalovirus
I Citomegalovirus (CMV)
Il citomegalovirus (CMV) è il più grande tra i virus erpetici umani, caratterizzato da un genoma a DNA a doppio filamento di circa 230.000–240.000 paia di basi.

Il parere di chi lo usa
"Riconosce in modo eccellente anche i termini tecnici (cosa rarissima) e la rielaborazione del testo è attenta e precisa. Molto superiore ad altre applicazioni provate in passato."
"Ha trascritto fedelmente ogni parola detta dal professore senza farsi confondere dai colpi di tosse o dal rumore di sottofondo. Ottimo strumento."
"Sbobina fatta benissimo nonostante la materia molto tecnica. Trasforma il parlato in un testo strutturato e senza l'utilizzo della prima persona. Utilissimo."
Creato da uno studente,
per tutti gli studenti.
Sbobby è nato da un bisogno reale: smettere di perdere ore a sbobinare manualmente per iniziare a studiare sul serio.
È lo strumento pensato per chi deve districarsi tra le lezioni più complesse e i tempi stretti della sessione.
Dietro ogni dettaglio c’è la consapevolezza di cosa significhi preparare un esame oggi.
Mauro
Studente di Medicina & Creatore di Sbobby
Prezzi Trasparenti
Nessun abbonamento, paghi solo per quello che usi.
A Consumo
Paga solo per quello che usi
Pacchetti Crediti
Risparmia con i pacchetti prepagati